Tel: +84 24 35742022 | Fax: +84 24 35742020
Tên kiến nghị: Một số vướng mắc về Thông báo số 1234/TB-ATTP ngày 19/4/2019 và Dự thảo Thông tư hướng dẫn Thực hành sản xuất tốt (GMP) trong sản xuất, kinh doanh thực phẩm bảo vệ sức khỏe
Tình trạng: Đã phản hồi
Đơn vị kiến nghị: Hiệp Hội Thương Mại Mỹ tại Việt Nam (AmCham Việt Nam) Địa chỉ: New World Hotel, Rm. 323, Fl.3, 76 Le Lai Str., Dist. 1, HCMC
Công văn: 1336/PTM - VP, Ngày: 18/06/2019
Nội dung kiến nghị:
Ngày 19/4/2019, Cục An toàn thực phẩm – Bộ Y tế ban hành văn bản số 1234/TB-ATTP hướng dẫn bổ sung Giấy chứng nhận GMP trong sản xuất, kinh doanh và đăng ký bản công bố sản phẩm TPBVSK, và đến tháng 5/2019 công bố dự thảo Thông tư Hướng dẫn GMP trong sản xuất, kinh doanh TPBVSK với hạn góp ý là 17/7/2019. Cả 2 văn bản này có rất nhiều bất cập về mặt thực tiễn cũng như về pháp lý, có thể gây ảnh hưởng rất lớn đến hoạt động của các doanh nghiệp kinh doanh TPBVSK tại Việt nam, cụ thể như sau:
Thông báo này quy định: Đối với TPBVSK nhập khẩu đã được cấp Giấy xác nhận công bố phù hợp quy định an toàn thực phẩm hoặc Giấy tiếp nhận đăng ký bản công bố sản phẩm còn hiệu lực
“2.1. Sản phẩm sản xuất trước ngày 01/07/2019 được tiếp tục nhập khẩu, lưu thông đến hết hạn sử dụng của sản phẩm
2.2. Sản phẩm sản xuất sau ngày 01/07/2019 tổ chức, cá nhân phải bổ sung giấy chứng nhận GMP của nhà sản xuất vào hồ sơ và thông báo về Cục An toàn thực phẩm trước khi nhập khẩu sản phẩm.”
Như vậy, với Thông báo số 1234/TB-ATTP, các sản phẩm TPBVSK mặc dù có giấy phép do Cục An toàn thực phẩm cấp còn hiệu lực, nếu sản xuất từ ngày 1/7/2019 trở đi sẽ không được tiếp tục nhập khẩu vào Việt nam nếu không kịp bổ sung gi ấy chứng nhận GMP. Hơn nữa, đây phải là giấy chứng nhận GMP cho TPBVSK, một giấy chứng nhận mà rất ít nước trên thế giới có, vì phần lớn các nước trên thế giới chỉ cấp giấy chứng nhận GMP cho thực phẩm nói chung hoặc dược phẩm.
Về thực tiễn, Thông báo này sẽ gây một cản trở rất lớn trong thương mại, rất nhiều sản phẩm đang nhập khẩu và kinh doanh bình thường sẽ không được nhập khẩu tiếp từ ngày 1/7/2019, vì 1) nước xuất khẩu không cấp giấy chứng nhận GMP cho TPBVSK, mà chỉ có giấy chứng nhận GMP hoặc tương đương cho thực phẩm hoặc dược phẩm; và 2) với một số nước có cấp GMP cho TPBVSK, thời gian từ nay đến 1/7/2019 là quá ngắn để các doanh nghiệp có thể hoàn tất các thủ tục bổ sung giấy chứng nhận GMP cho TPBVSK.
Về pháp lý, Thông báo này cũng trái với quy định của Nghị định 15/2018/NĐ-CP, vì:
- Thông báo số 1234/TB-ATTP cho rằng “Căn cứ pháp lý Điểm đ Khoản 1, Điểm đ Khoản 2 Điều 7 và Khoản 3 Điều 28 Nghị định số 15/2018/NĐ-CP”. Điểm đ Khoản 1 Điều 7 quy định “hồ sơ đăng ký công bố bản công bố sản phẩm đối với thực phẩm nhập khẩu cần có…đ) Giấy chứng nhận cơ sở đủ điều kiện an toàn thực phẩm đạt yêu cầu Thực hành sản xuất tốt (GMP) hoặc chứng nhận tương đương trong trường hợp sản phẩm nhập khẩu là TPBVSK áp dụng từ ngày 1/7/2019”. Điểm đ Khoản 2 Điều 7 quy định về hồ sơ đăng ký công bố bản công bố sản phẩm đối với thực phẩm sản xuất trong nước nên chúng tôi không nhắc đến tại đây. Khoản 3 Điều 28 quy định “Kể từ ngày 01 tháng 07 năm 2019, các cơ sở sản xuất thực phẩm bảo vệ sức khỏe phải áp dụng Thực hành sản xuất tốt (GMP) thực phẩm bảo vệ sức khỏe theo hướng dẫn của Bộ Y tế”.
- Như vậy, Điểm đ Khoản 1 điều 7 Nghị định 15 là quy định cho thành phần hồ sơ đăng ký đối với thực phẩm nhập khẩu, và chỉ áp dụng cho những sản phẩm nộp đăng ký từ 1/7/2019 trở đi chứ không áp dụng cho các sản phẩm đã đăng ký trước đó. Điều 28 là nói đến các cơ sở “sản xuất” chứ không nói đến cơ sở “nhập khẩu”, “kinh doanh”. Tuy nhiên, Thông báo số 1234/TB-ATTP lại mặc nhiên quy định đối với các lô hàng thực phẩm nhập khẩu đã được cấp Giấy Đăng ký bản công bố sản phẩm còn hiệu lực sẽ không được nhập khẩu từ ngày 1/7/2019 nếu không bổ sung giấy chứng nhận GMP cho TPBVSK. Điều này là không có cơ sở pháp lý và gây cản trở cho hoạt động kinh doanh bình thường của doanh nghiệp.
- Tại Điều 42 Nghị định 15 quy định “Các sản phẩm đã được cấp Giấy tiếp nhận bản công bố hợp quy và Giấy xác nhận công bố phù hợp quy định an toàn thực phẩm trước ngày Nghị định này có hiệu lực được tiếp tục sử dụng đến khi hết thời hạn ghi trên giấy và hết thời hạn sử dụng của sản phẩm.” Như vậy, với các sản phẩm đăng ký theo Nghị định 38, Chính phủ trong Nghị định 15 còn cho phép được tiếp tục nhập khẩu, lưu hành khi giấy phép còn hiệu lực, thì không có lý do gì Thông báo số 1234/TB-ATTP lại cấm nhập khẩu kể từ ngày 1/7/2019 các mặt hàng có giấy phép còn hiệu lực, kể cả giấy phép cấp theo Nghị định 38, hay mới cấp theo Nghị định 15, chỉ vì không bổ sung được giấy chứng nhận GMP cho TPBVSK, mà cho đến bây giờ Bộ y tế còn chưa ban hành Thông tư hướng dẫn về giấy chứng nhận này (mới ở dạng dự thảo).
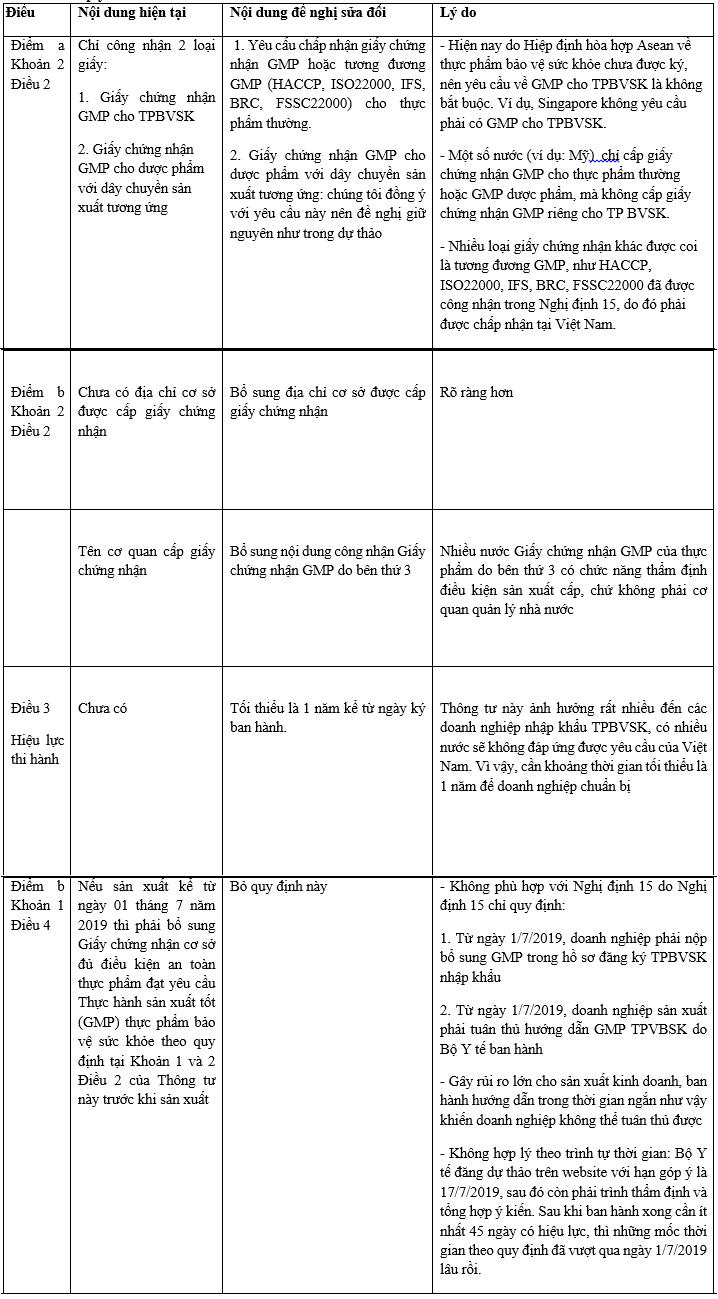
Vì vậy, Amcham kính đề nghị Bộ Y tế xem xét điều chỉnh lại Thông báo số 1234/TB-ATTP như sau để đảm bảo tuân thủ Nghị định 15/2018/NĐ-CP và không gây cản trở cho hoạt động kinh doanh bình thường của doanh nghiệp:
Về quy trình ban hành Thông tư: Do trong dự thảo có những mốc thời gian không phù hợp với quy đị nh của pháp luật nên chúng tôi rất lo lắng về quy trình ban hành. Đề nghị Bộ Y tế áp dụng đúng quy định ban hành văn bản quy phạm pháp luật tại Luật Ban hành văn bản quy phạm pháp luật 2015 số 80/2015/QH13, điều 101 “Trong quá trình soạn thảo thông tư, bộ, cơ quan ngang bộ chủ trì soạn thảo phải lấy ý kiến đối tượng chịu sự tác động tr ực tiếp của văn bản; nêu những vấn đề cần xin ý kiến phù hợp với từng đối tượng lấy ý kiến và xác định cụ thể địa chỉ tiếp nhận ý kiến; đăng tải toàn văn dự thảo trên Cổng thông tin điện tử của Chính phủ và cổng thông tin điện tử của bộ, cơ quan ngang bộ trong thời gian ít nhất là 60 ngày” và Điều 151 “Thời điểm có hiệu lực của toàn bộ hoặc một phần văn bản quy phạm pháp luật được quy định tại văn bản đó nhưng không sớm hơn 45 ngày kể từ ngày thông qua hoặc ký ban hành đối với văn bản quy phạm pháp luật của cơ quan nhà nước trung ương”.
Đơn vị phản hồi: Bộ Y tế
Công văn: 2233/ATTP - SP; 2443/ATTP - NĐTT, Ngày: 15/07/2019
Nội dung trả lời:
Ngày 02/2/2018 Chính phủ nước Công hòa x'ã hội chủ nghĩa Việt Nam đã ban hành Nghị định số 15/2018/NĐ-CP quy định chi tiết thi hành một số điều của Luật An toàn thực phẩm. Theo đó, Điểm d Khoản 1, Điểm đ khoản 2 Điều 7 đã quy định trong hồ sơ đăng ký bản công bố sản phẩm đối với thực phẩm bảo vệ sức khỏe nhập khẩu và sản xuất trong nước phải có giấy chứng nhận cơ sở đủ điều kiện an toàn thực phẩm đạt yêu cầu Thực hành sản xuất tốt (GMP) áp dụng từ ngày 01/07/2019. Trước đó, ngày 08/08/2016 Bộ Y tế đã ban hành quyết định số 4288/QĐ - BYT ban hành tài liệu hướng dẫn thực hành sản xuất tốt (GMP) thực phẩm bảo vệ sức khỏe (Health Supplements). Việc áp dụng thực hành sản xuất tốt (GMP) đối với thực phẩm bảo vệ sức khỏe nhằm đảm bảo chất lượng của sản phẩm cũng như quyên lợi của người tiêu dùng.
Về thực tiễn, ngày 08/8/2Ọ1Ố Quyết định, số 4288/QĐ-BYT nêu trên được ban hành, các tổ chức, cá nhân đã oó 2 năm 9 tháng để tỉếp cận thông tin nội dung kỹ thuật của thực hành sản xuất tốt (GMP) thực phẩm bảo vệ sức khỏe. Tiếp theo, từ ngày 02/02/2018, Nghị định số 15/2018/NĐ - CP có hiệu lực đến nay là 1 năm 4 tháng để các tổ chức, cá nhân có thời gian chuẩn bị thực hiện quy định bắt buộc áp dụng thực hành sản xuất tốt (GMP) thực phẩm bảo vệ sức khỏe. Với thời gian lộ trình chuẩn bị như trên, việc thực hiện quy định của Chính phủ không gây cản trở cho hoạt động sản xuất, kinh doanh.
Về pháp lý căn cứ theo Khoản 3 Điều 28 Nghị định số 15/2018/NĐ-CP, kể từ ngày 01 .tháng 07 năm 2019, các cợ sở sản xuất thực phản bảo vệ sức khỏe phải áp dụng Thực hành sản xuất tốt (GMP) thực phẩm bảo vệ sức khỏe theo hướng dẫn của Bộ Y tế. Quy định này sẽ được áp dụng công bằng giữa sản xuất trong nước và nhập khẩu để đảm bảo nguyên tắc không phân biệt đối xử của WTO.
về điều kiện chuyển tiếp, cắn cứ Điều 42 Nghị định số 15/2018/NĐ-CP, các sản phẩm đã được cấp Giấy tiếp nhận bản công bố hợp quy và Giấy xác nhận công bố phù họp quy định an toàn thực phầm trước ngày 02/2/2018 được tiếp tục sử dụng đến khì hết thời hạn ghi trên giấy và hết thời hạn sử dụng của sản phẩm, Đồng thời, theo Khoản 3 Điều 28, kể từ ngày 01 tháng 07 năm 2019 các cơ sử sản xuất thực phẩm bảọ vệ sức khỏe phải áp dụng Thực hành sản xuất tốt (GMP) thực phẩm bảo vê sức khỏe theo, hướng dẫn của Bộ Y tế, Như vậy, các sản phẩm thực phẩm bảo vệ sực khỏe đã được Gấp Giậy tiếp nhận bản công bố hợp quy và Giấy xác. nhận công bố phù hợp quy định an toàn thực phẩm còn hiệu lực không phải công bố lại mà chi cần bổ sung Giấy chứng nhận thực hành sản xuất tốt (GMP) nếu sản phẩm đó (sản xuất sau ngày 01/7/2019) được tiếp tạo nhập khẩu vào Việt Nam, Đối vói những cơ sở sản xuất không đáp ứng GMP, Thông báo 1234/TB-ATTP đã có hướng đẫn cụ thể việc thay đổi nhà sẳn xuất.
Qụy định cụ thể về Giấy chứng nhận tương đương GMP đối với ứiựo phẩm bảo vệ sức khỏe sễ được Bộ Y tễ quy định cụ thể trong Thông tư hướng dẫn Thực •hành sản xuất tốt (GMP) trong sản xuất, kỉnh doanh thực phẩm bảo vệ sức khỏe.
Các góp ý của Hiệp hội Thương mại Mỹ tại Việt Nam. đối với việc xây đựng Thông tư hướng dẫn Thực hành sản xuất tốt (GMP) trong sản xuất, kinh doanh thực phẩm bảo vệ sức khỏe:
1 Góp ý về quy trình ban hành Thông tư:
+ Quy trình xây dựng Thông tư hướng dẫn Thực hành sản xuất tốt (GMP) trong sản xuất, kinh doanh thực phẩm bảo vệ sức khỏe được thực hiện theo quy định tại Thông tư số 22/2014/TT-BYT ngày 30/6/2014 của Bộ Y tế quy định việc soạn thảo, ban hành và tổ chức triển khai thi thành văn bản quy phạm pháp luật về y tế. Việc lấy ý kiến rộng rãi dự thảo Thông tư được tiến hành từ ngày 16/5/2019 và Bộ Y tế đã ban hành Thông tư số 18/2019/TT-BYT ngày 17/7/2019 về hướng dẫn Thực hành sản xuất tốt (GMP) trong sản xuất, kinh doanh thực phẩm bảo vệ sức khỏe. Như vậy thời gian lẩy ý kiến góp ý là 61 ngày.
+ Đối với hiệu lực thi hành: Nghị định số 15/2018/NĐ-CP có hiệu lực thi hành từ ngày 02/02/2018 đến nay là 01 năm 4 tháng để các tổ chức, cá nhân có thời gian chuẩn bị thực hiện quy định bắt buộc áp dụng thực hành sản xuất tốt (GMP) thực phẩm bảo vệ sức khỏe. Với thời gian lộ trình chuần bị như trên, việc thực hiện quy định của Chính phủ không gây cản trở cho hoạt động sản xuât, kinh doanh của doanh nghiệp và việc ban hành Thông tư số 18/2019/TT- BYT có hiệu lực ngay để thuận lợi cho doanh nghiệp áp dụng và triển khai thực hiện.
góp ý về dự thảo nội dung Thông tư:
+ Đối với giấy chứng nhận tương đương và nội dung củạ giấy chứng nhận cơ sở đủ điều kiện an toàn thực phẩm đạt yêu cầu GMP đối với thực phẩm bảo vệ sức khỏe nhập khẩu đã được quy định cụ thể tại Khoản 1, Khoản 2 Điều 4 Thông tư số 18/2019/TT-BYT.
+ Đối với góp ý về việc bổ sung bản sao có xác nhận của cơ sở đối với Giấy chứng nhận Cơ sở đủ điều kiện an toàn thực phẩm đạt yêu cầu thực hành sản xuất tốt (GMP) thực phẩm bảo vệ sức khỏe kể từ ngày 01/7/2019 đã được quy định tại Khoản 3, Điều 28 Nghị định số 15/2018/NĐ-CP của Chính phủ và được quy định cụ thể tại Điểm b, Khoản 1, Điều 6 Thông tư số 18/2019/TT- BYT của Bộ Y tế.